В мир науки тяжелая вода вошла не так давно, но сумела сразу привлечь к себе пристальное внимание. Почти за 100 лет исследований удалось выявить все ее основные свойства, благодаря которым ученые быстро нашли жидкости применение и научились ее производить. Многие вопросы, касающиеся воздействия воды на окружающий мир, остаются открытыми, из-за чего интерес к ней не пропадает до сих пор.

История открытия
Ученый Г. Юри проявлял неподдельный интерес по отношению к ядерной структуре веществ. Именно это привело к выдвижению им теории о том, что при разделении водорода можно получить новые виды его изотопов, о существовании которых некогда говорил Э. Резерфорд.

Под руководством Г. Юри в 1932 году был проведен эксперимент. Его суть заключалась в искусственном выпаривании 6 л водорода. Результатом стало получение остатка объемом 3 см³, который помог выявить формулу тяжелой воды и подтвердил теорию о ее существовании. А в 1933 году другой ученый Г. Льюис провел свой эксперимент. Он сумел получить нужные изотопы высокой концентрации путем электролиза обычной воды, что привлекло к этому явлению много внимания со стороны физиков во всем мире.

Интересно! Объем тяжелой воды от общей массы H₂O на Земле составляет всего лишь 0,02%.
Описание и основные свойства
Тяжелую воду также называют оксидом дейтерия. Именно этот компонент делает ее уникальной. По химической формуле тяжелая вода отличается от обычной только тем, что вместо атомов водорода в ней присутствуют тяжелые изотопы, которые и называются дейтерием, с массовым числом 2. Ее записывают в виде D₂O или 2H₂O.

Как и у обычной воды, у оксида дейтерия отсутствует цвет, вкус или запах. Но разница между ними все же есть не только в формуле. Основные свойства тяжелой воды делают ее уникальной и заметно отличающейся от привычной человеку жидкости.

Наибольшее значение имеют следующие параметры:
- температура закипания – 101,43 °C,
- температура кристаллизации – 3,813 °C,
- плотность (при 25 °C) – 1,1042 г/см³,
- молекулярная масса – 20,034 г/моль,
- давление паров (при 13,1 °C) – 10 мм рт. ст.,
- критическое давление – 31,86 МПа.

Плотность тяжелой воды, высокая прочность связи и масса ее молекул способствуют тому, что она активнее удерживается в жидкой фазе, обладает повышенной на 20% вязкостью, и все реакции с ней протекают значительно медленнее.

Физиологическое воздействие
С момента открытия оксида дейтерия было проведено множество экспериментов, доказавших его серьезное воздействие на окружающий мир и живые организмы. Вода токсична лишь в слабой степени, но производит угнетающий эффект. Он приводит к заметному замедлению всех биологических процессов. Например, микробы и бактерии прекращают размножаться, водоросли, грибы и ткани животных перестают расти, а растения вянут.

Однако снижение доли дейтерия может вызывать даже положительный эффект. Эксперименты показали, что при 50% концентрации жидкость способна оказать антимутагенный эффект, простимулировать увеличение массы, ускорить развитие половых органов, привести к повышению количества семян у растений и даже вызвать сперматогенез у птиц. Снижение оксида дейтерия до 25% приводит к повышению стерильности организма и минимизирует негативное воздействие.

Проводимые эксперименты касались даже раковых опухолей. Протестированная на группе мышей жидкость привела к уменьшению опухолей, но вместе с этим погибли сами животные. Позже ученые попробовали применить облегченный вариант оксида, который немного снизил размеры новообразований, но сохранить жизнь испытуемым все равно не удалось. Физическое угнетение оказывается чересчур значительным, чтобы подавить опухоль, не затронув само живое существо.

Считается, что удаление дейтерия из воды, с которой контактируют люди, могло бы повысить активность человеческого тела и мозга, а также продлить срок жизни. Но нарушение природного баланса может привести к непоправимым последствиям не только для человека, но и для многих других организмов и растений. Поэтому подобные вопросы перестали рассматриваться много лет назад.
Справка! Человек может выпить целый стакан тяжелой воды и не испытать на себе никакого негативного воздействия. Дейтерий выйдет из организма через несколько дней.
Получение
Молекулы оксида дейтерия присутствуют во всей воде, с которой приходится контактировать людям. Но считается, что в чистом виде в природе их практически нет, а встречающиеся имеют несколько иную, ослабленную формулу – HDO.
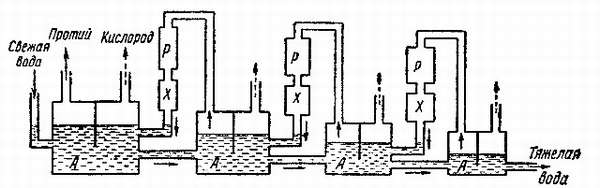
Получить оксид дейтерия довольно тяжело. Процедура его изготовления недостаточно технологична, из-за чего финансовые затраты остаются колоссальными. Требования к составу жидкости, применяемой в промышленности, довольно строгие. На соответствие качеству приходится тратить дополнительные средства и силы. Результатом становится дороговизна и дефицит, которые мешают исследованиям и открытиям новых свойств жидкости.
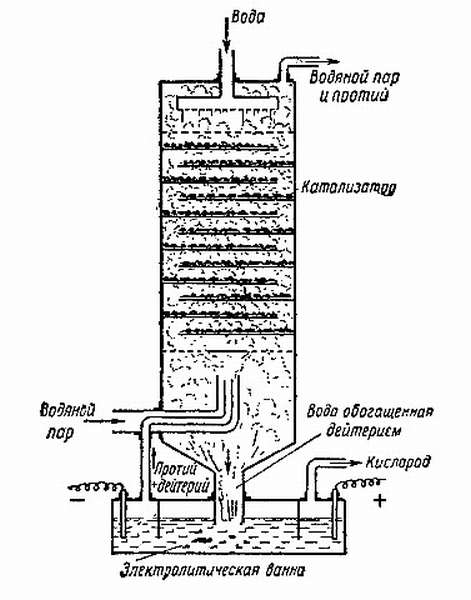
Для создания тяжелой жидкости применяется метод электролиза. Он представляет собой разложение вещества на составляющие путем проведения его через электрический ток. При электролизе H₂O испаряется, а D₂O накапливается. При дальнейшей фракционной перегонке возможно получение чистого оксида дейтерия. На создание 1 кг тяжелой жидкости тратится около 60 тыс. кВт⋅ч электроэнергии, что равнозначно затратам на выплавку 3 тонн алюминия. Именно этим обусловлена высокая стоимость такой воды.
Применение
Изначально изотопы тяжелой воды не применялись нигде, кроме проводимых экспериментов. Но через некоторое время глазам ученых открылись новые возможности этого оксида, которые вскоре были реализованы на практике. Основными сферами применения стали наука и промышленность.

Где используют такую воду:
- ядерные технологии – способствует торможению нейтронов и играет роль теплоносителя,
- химия, биология, физика, гидрология – применяется в качестве изотопного индикатора и детектора нейтрино,
- медицина – проводятся научные исследования, которые показывают потенциал применения оксида для лечения некоторых болезней.

При более подробном изучении оксида дейтерия могут быть открыты его новые свойства. Это поможет найти новое применение его молекулам.
Виды тяжелой жидкости
Существует несколько видов тяжелой воды. Они отличаются друг от друга химическим составом и основными свойствами. Некоторые из них до сих пор остаются малоизученными, что связано со сложностью проведения экспериментов.

Вторым видом после обычной тяжелой жидкости считается полутяжелая – DHO. Именно она встречается в природе. Главное отличие от обычной тяжелой воды заключается в том, что у нее только один атом заменяется дейтерием, а второй остается водородом. В реальности она состоит из смеси DHO, D₂O и H₂O.

Третий вид – сверхтяжелая вода (T₂O). Ее главным отличием стало присутствие трития, из-за которого полностью меняются все свойства жидкости. Закипание сверхтяжелой воды происходит при 104 °C, замерзает она при 9 °C, а ее плотность составляет 1,21 г/см³. При этом она радиотоксична.

Также существует 48 подвидов, где один из атомов воды заменен тяжелым изотопом. 39 из них являются радиоактивными. Наиболее популярной из них стала тяжелокислородная вода с замененным изотопом 16O на 17O или 18O. Она применяется для исследований онкологических заболеваний.

Исследования тяжелой воды остаются актуальными до сих пор. Особые свойства позволяют применять ее в важных сферах, где она становится практически незаменимой. При дальнейших экспериментах возможно выявление новых особенностей этой жидкости. Не исключено, что они приведут к научным прорывам и новым открытиям.